- ハンルイグループ
- 品質
- 研究開発
- 製造販売と安定供給
江蘇恒瑞医薬は
中国医薬品業界の
リーディングカンパニーです。
江蘇恒瑞医薬(Jiangsu Hengrui Pharmaceuticals Co., Ltd.)は1997年に設立。主に抗がん剤・麻酔薬・造影剤の研究・開発及び製造を行っており、上海証券取引所に上場しています。
売上推移・構成
*表を左右にスライドしていただくと続きが見れます。
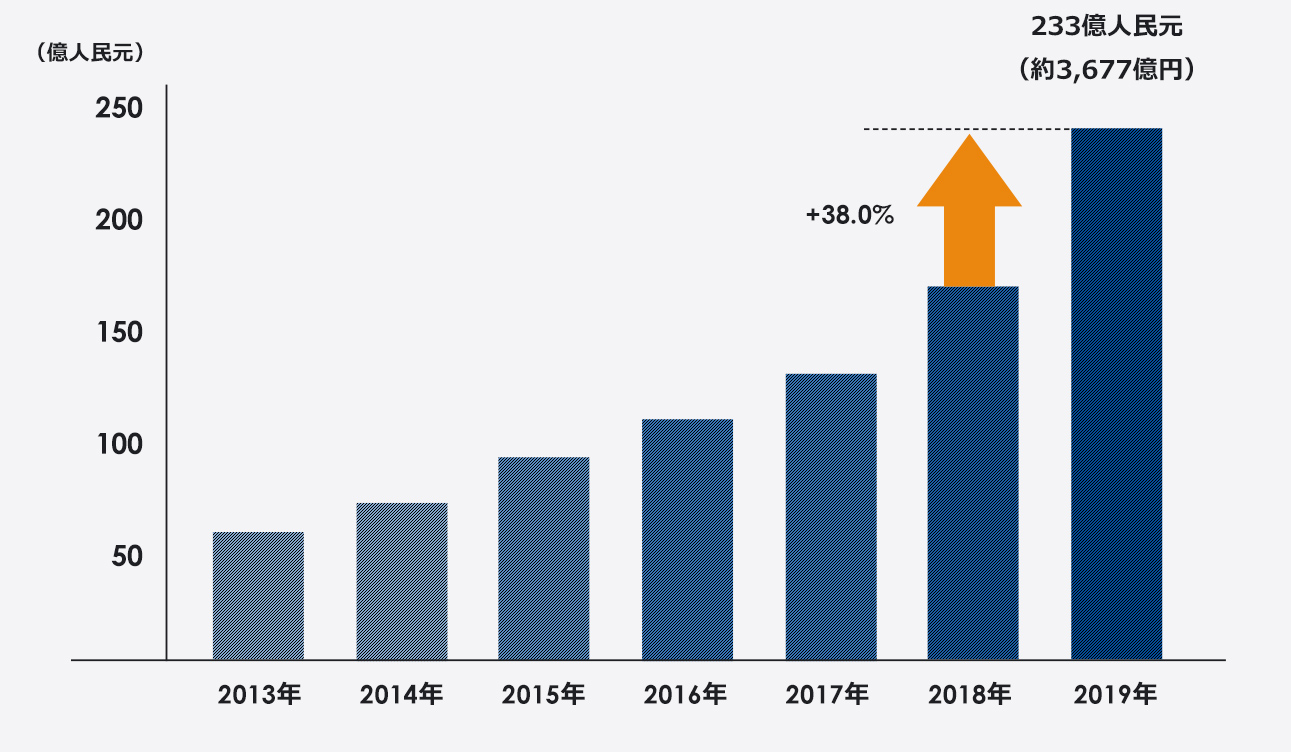
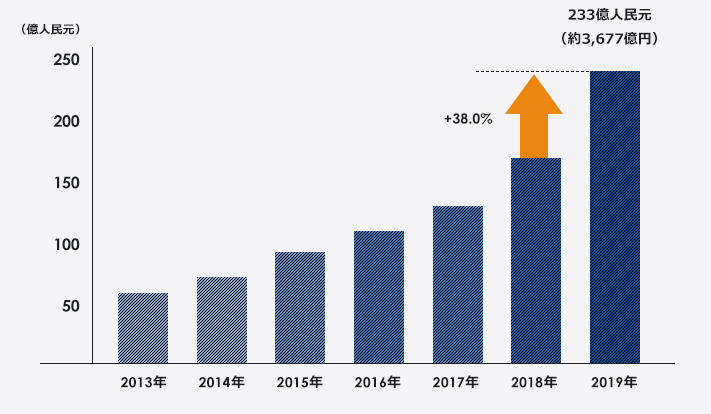
2019年の医薬品製造販売業のみの売上は232.5億元(約3,669億円)
※日本円の金額は2019年の年間平均レート(1元=15.78円)で換算
2019年売上構成
ジェネリック医薬品を中心に、
抗がん剤の分野で
世界から高い評価を受けています
江蘇恒瑞医薬の製品は、現在、抗がん剤の売上げが全体の4割を占めています(抗がん剤45%、麻酔薬24%、造影剤14%)。 中国市場だけでなく、米国市場では2012年に、欧州市場では2014年にジェネリック抗がん剤が上市するなど、国際的に高い評価と信頼を獲得しています。日本でも2014年の日本法人設立以後、ジェネリック抗がん剤を中心に製造販売承認申請を行っており、2015年にはイリノテカン塩酸塩点滴静注液の製造販売承認を取得しました。
領域別
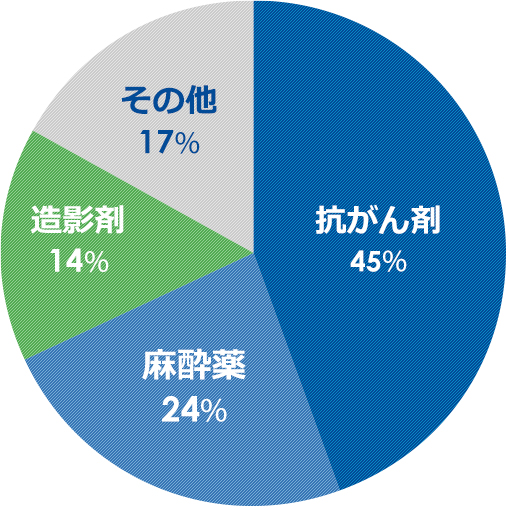
| 領域 | 売上 | 売上比率 |
|---|---|---|
| 抗がん剤 | 1,669億円 | 45% |
| 麻酔薬 | 869億円 | 24% |
| 造影剤 | 510億円 | 14% |
| その他 | 621億円 | 17% |
| 計 | 3,669億円 | 100% |
スタッフ構成
中国国内はもとより海外からも広く優秀な人材を登用。およそ25,000人のスタッフが本社のある連雲港をはじめ、世界各地で活躍しています。
- ・営業スタッフは14,500人強。中国国内の販売網は32の省・自治区・直轄市の病院や施設をカバー。
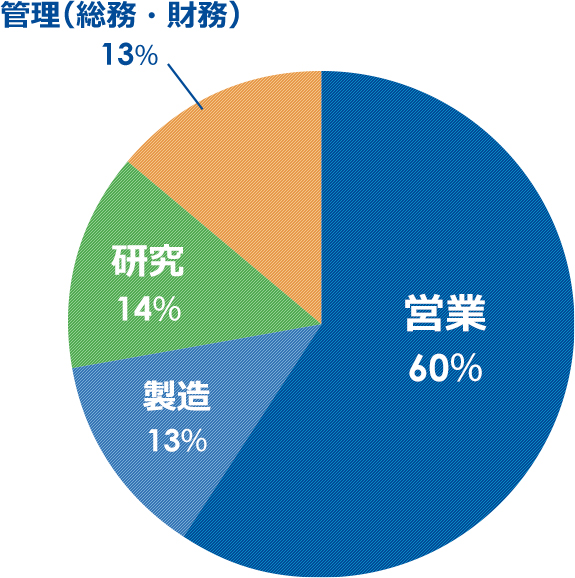
| 部門別 | 人数 |
|---|---|
| 営業 | 14,686人 |
| 製造 | 3,226人 |
| 研究 | 3,442人 |
| 管理(総務・財務) | 3,077人 |
| 計 | 24,431人 |
グローバルに活躍するハンルイグループ
連雲港・上海・成都に生産拠点を設けているほか、R&Dセンター、子会社、関連会社などを世界各地に配し、確固たる地位と信頼を築いています。
- Lianyungang, CHINA
-
- Jiangsu Hengrui Pharmaceuticals[Headquarters]
- Jiangsu Hengrui Medicine Sales
- Jiangsu Singch Pharmaceuticals
- Jiangsu Suncadia Pharmaceuticals
- Shanghai, CHINA
-
- Shanghai Hengrui Pharmaceuticals
- Shanghai Suncadia Pharmaceuticals
- Suz hou, CHINA
-
- Suzhou Suncadia Biopharmaceutical
- Suzhou Callisyn Biopharmaceutical
- Chengdu, CHINA
-
- Chengdu Suncadia Pharmaceuticals
- Chengdu Xinyue Medicine
- Beijing, CHINA
-
- Beijing Hengseng innovative
- Pharmaceutical Technology
- Hong Kong, CHINA
- Hong Kong Ogilvy Health Management
- New Jersey, USA
- Hengrui(USA)
- Nagoya, JAPAN
- Hengrui Medical Japan
- Willich, GERMANY
- Cadiasun Pharman GmbH
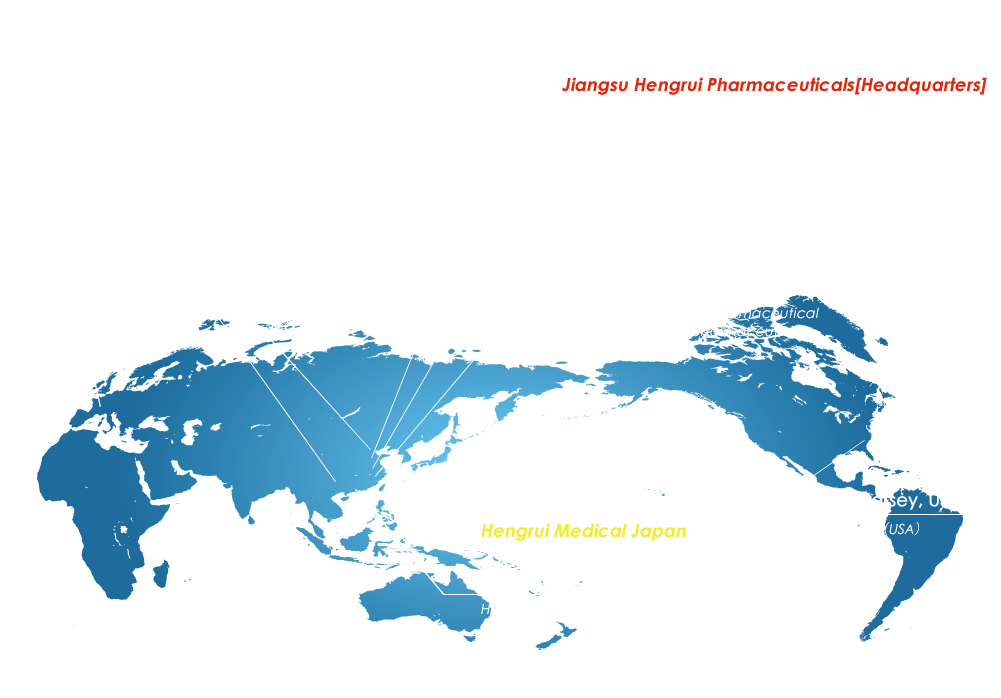
江蘇恒瑞医薬は
日本、米国、欧州でGMP認証を取得した
「世界品質の医薬品」を供給
■GMPとは(参考) 厚生労働省 後発医薬品広報資料
Good Manufacturing Practiceの略。
医薬品及び医薬部外品の品質確保を図るため、原料の受入れから最終製品の包装、出荷に至るまで、全製造工程における組織的な管理に基づく品質保証体制を確立するために定められた基準(医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令)
「ジェネリック医薬品への疑問に答えます ~ジェネリック医薬品Q&A~」
原薬の承認状況
世界をマーケットに
高品質の医薬品をお届けしています。
日本、米国、欧州などで注射剤・経口剤・原薬の製造・販売の承認を取得し、グローバルに展開しています。
- 厚生労働省
- ・Irinotecan HCl
- ・Letrozole
- ・Oxaliplatin
- ・Sevoflurane
- ・Dexmedetomidine HCl
- EDQM
- ・Caspofungin Acetate
- ・Etoposide
- ・Ifosfamide
- ・Iodixanol
- ・Letrozole
- ・Oxaliplatin
- ・Sevoflurane
- FDA
- ・Atracurium Besylate
- ・Cisatracurium Besylate
- ・Carmustine
- ・Caspofungin Acetate
- ・Dexmedetomidine HCl
- ・Docetaxel Trihydrate
- ・Etoposide
- ・Gadoteric Acid Meglumine
- ・Gadobutrol
- ・Irinotecan HCl
- ・Ifosfamide
- ・Ioversol
- ・Iodixanol
- ・Letrozole
- ・Oxaliplatin
- ・Sevoflurane
- ・Tolvaptan
- ・Trabectedin
製剤の承認状況
- 厚生労働省
- ・Letrozole Tab.
- ・Irinotecan HCl Inj.
- ・Dexmedetomidine HCl Inj.
- EDQM
- ・Caspofungin Acetate for Inj.
- ・Cyclophosphamide for Inj.
- ・Desflurane, Liquid for Inhalation
- ・Letrozole Tab.
- ・Oxaliplatin for Inj.
- ・Sevoflurane Inhalation
Anesthetic - ・Iodixanol Inj.
- ・Ivabradine Sulfate Tab.
- FDA
- ・Daptomycin for Inj.
- ・Cisatracurium Besylate Inj.
- ・Cyclophosphamide for Inj.
- ・Dexmedetomidine HCl Inj.
- ・Dexmedetomidine HCl Inj.
(RTU) - ・Docetaxel Inj.
- ・Docetaxel Inj. (2-vial)
- ・Gabapentin Cap.
- ・Irinotecan HCl Inj.
- ・Letrozole Tab.
- ・Oxaliplatin Inj.
- ・Sevoflurane Inhalation
Anesthetic - ・Caspofungin Acetate for Inj.
- ・Cisatracurium Besylate Inj.
(preservative) - ・Desflurane, Liquid for Inhalation
- ・Thiotepa for Inj.
- ・Fondaparinux Sodium Inj.
※FDA(米国)、EDQM(欧州)
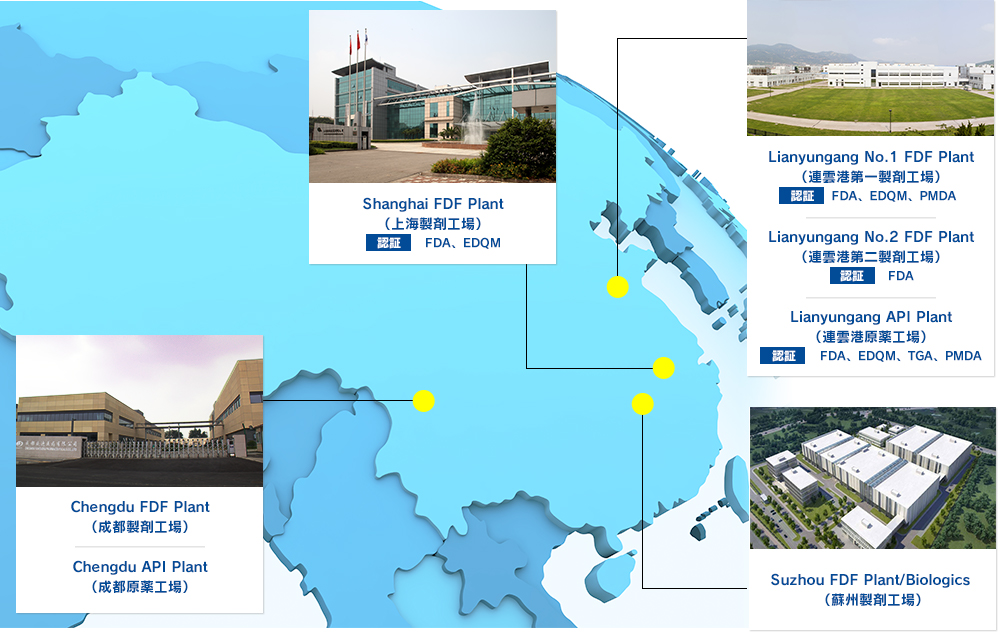
原薬から製剤まで一貫製造
江蘇恒瑞医薬の製造力は中国最大規模
中国各地に点在する製造サイトはいずれも高度な生産システムを備え、
原薬から製剤までの高品質な製品の供給を可能にしています。
日本向け製品もこれらの工場で造られています。
*表を左右にスライドしていただくと続きが見れます。
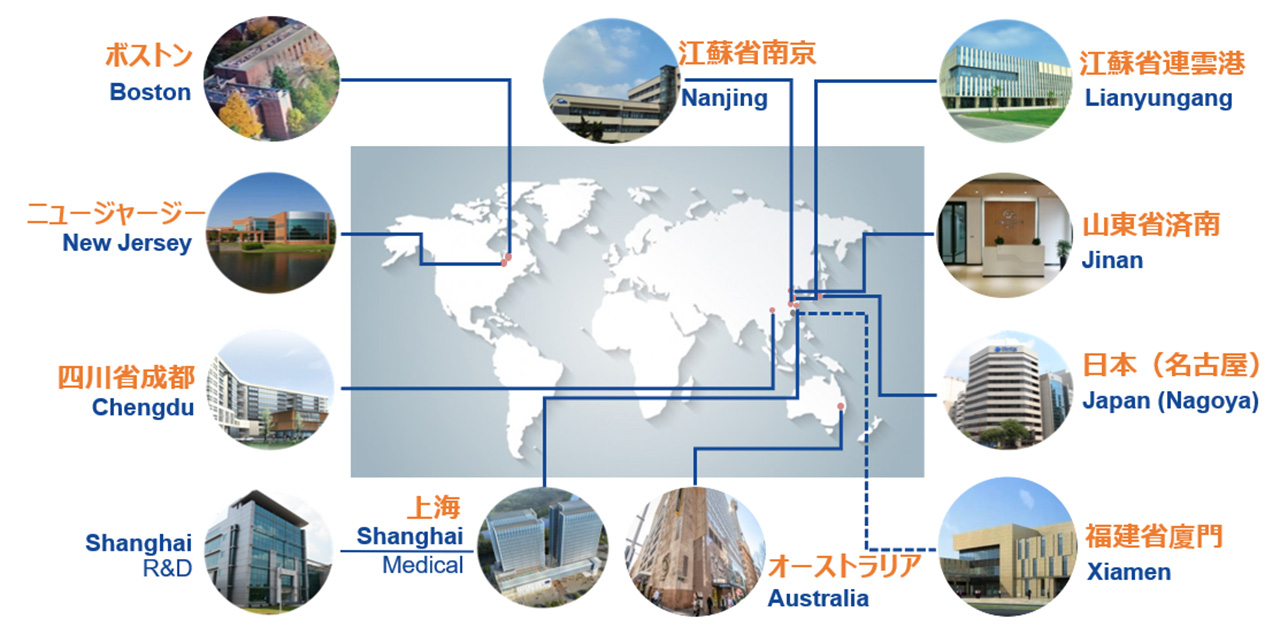
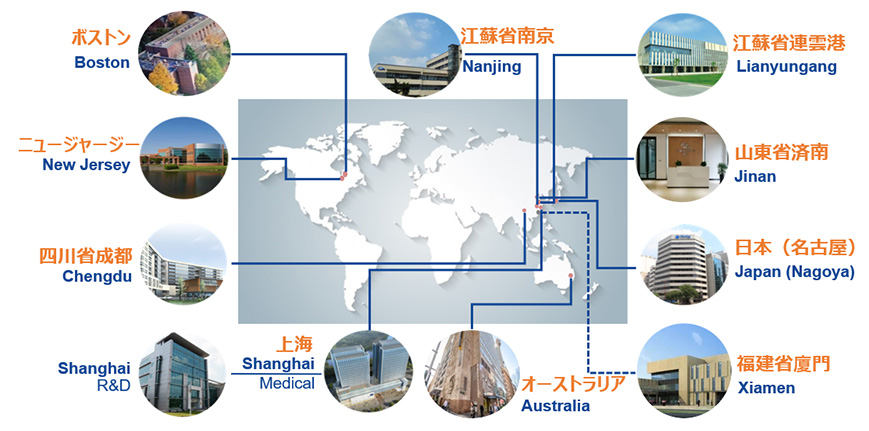
海外にも研究拠点を設置。
新薬の研究・開発も積極的に推進。
R&Dセンター
世界中からスタッフを登用。現在、研究・開発の拠点を連雲港・上海・成都に加え米国にも設置し、臨床試験の拠点も設けています。
*表を左右にスライドしていただくと続きが見れます。
研究開発費
江蘇恒瑞医薬は年間売上の約15%を研究・開発に投入。新薬の開発にも積極的に取り組み、中国国内で承認取得済みが5件、開発中の品目も多数あり、主にがん、内分泌、循環器、免疫の領域を扱っています。さらに、約500件の特許を所有し、そのうちの約300件がPCT(Patent Cooperation Treaty:特許協力条約)に基づく国際特許となります。(2019年現在)
*表を左右にスライドしていただくと続きが見れます。
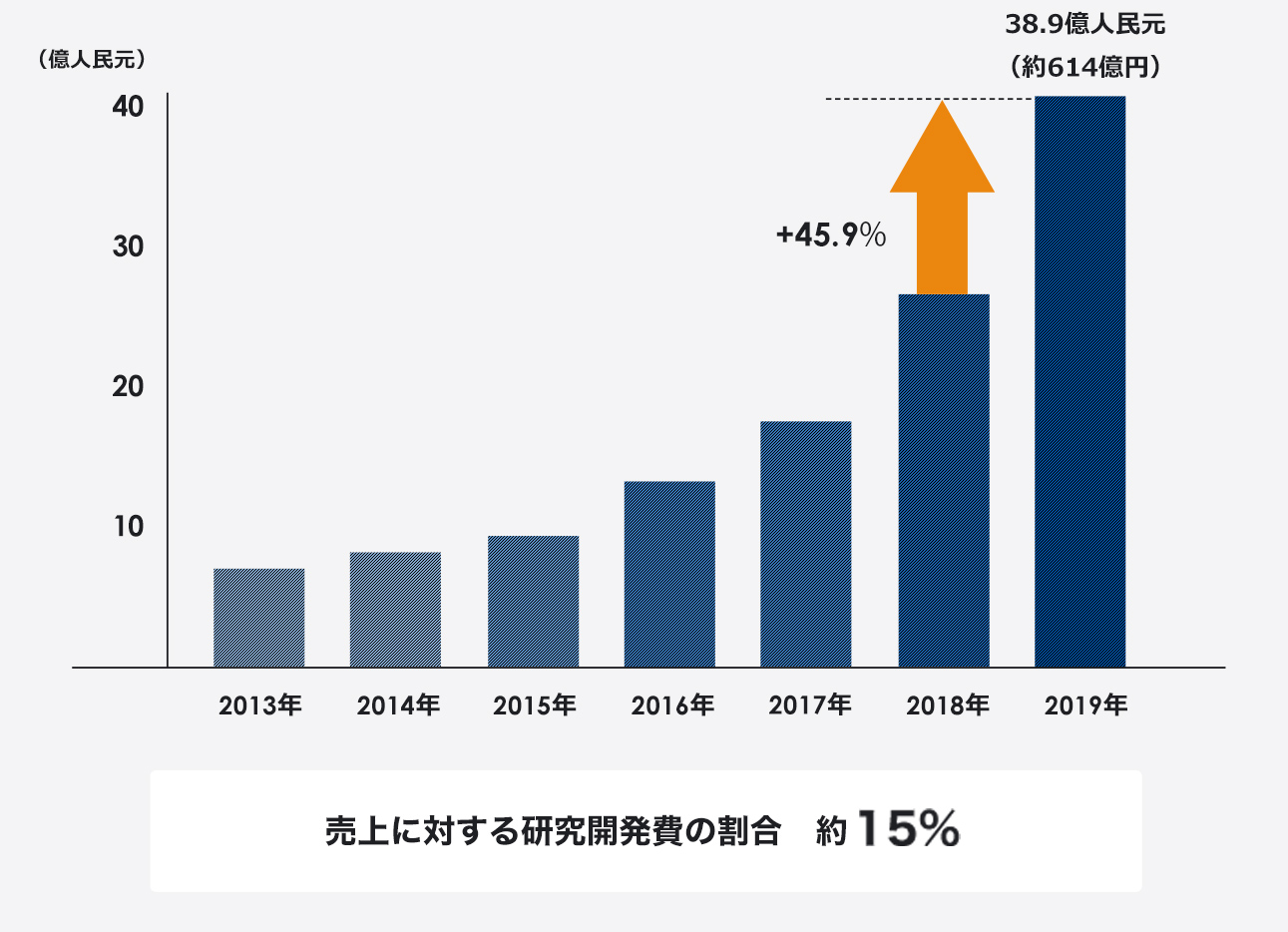
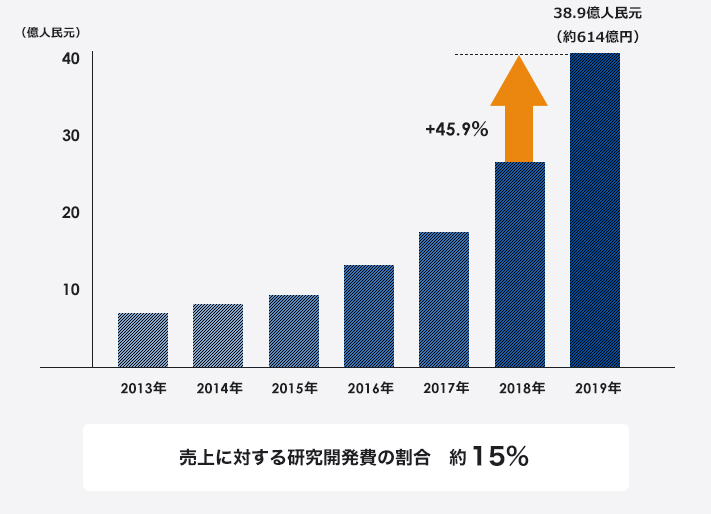
※日本円の金額は2019年の年間平均レート(1元=15.78円)で換算
ハンルイグループでは、専門知識を有するメンバーでチームを構成し、
日本国内での承認申請を行っています。
日本のスタッフも積極的に参加し、
日本市場で求められる高い品質を備えた製品を販売すべく、
中国本社と密にコミュニケーションを取りながらプロジェクトを進めています。
日本向け製品の製造販売・安定供給
日本の医薬品業界を熟知した経験豊富なスタッフが、日本市場のニーズに合わせたサービスを提供しています。
安定供給体制
中国で製造した製品は輸入後、国内製造所にて検品・包装を行い、全国の卸を介して医療機関へ速やかに納品されます。ガイドラインに従った社内ルールにもとづき、在庫管理も徹底しています。また、製造所とも第三者を介さず直接やりとりを行い、万一の場合に備え、すぐに製造・輸入の調整ができる体制を整えています。
信頼性保証体制


製造販売後も製品の品質・安全性を
適正に管理しています
ハンルイ医薬株式会社は医薬品製造販売業者として日本の法令を遵守し、製品の品質・安全性を管理し、必要な情報を迅速に提供できる体制を確立しています。
・品質保証
GQP省令(医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令)に従い、製品の品質管理が適正に実施されていることを日本のスタッフが定期的に監査し、製品の品質が確保されていることを保証いたします。
・安全管理
GVP省令(医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令)に従い、国内外の安全性情報を収集・評価し、製品を安全かつ適正に使用していただくための情報を迅速に提供いたします。


